Новости
Исследователи из Университета Саутхэмптона, являющиеся частью международной группы, помогли создать молекулу, которая доставляет в раковые клетки ионы натрия и хлора, что приводит к самоуничтожению канцерогенных клеток.
Переносчики синтетических ионов создавались и ранее, однако, именно последний вариант стал первым, который продемонстрировал то, как доставка соли в клетки вызывает их смерть. Такие ионные транспортеры, описанные в журнале Nature Chemistry, могут, по мнению ученых, помочь в разработке новых антираковых препаратов, которые бы оказались полезными и для пациентов с муковисцидозом.
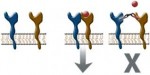
По утверждению одного из авторов исследования, профессора Филипа Гейла из Университета Саутхэмптона, проведенное исследование показывает то, как транспортеры хлорида могут действовать совместно с натриевыми каналами в клеточных мембранах, чтобы вызывать приток соли в клетку и последующую клеточную смерть.
Клетки человеческого организма поддерживают постоянную концентрацию ионов внутри клеточных мембран, а нарушение такого баланса может вызвать клеточный апоптоз, то есть запрограммированную клеточную смерть. При помощи такого механизма организм избавяется от повреждненых или опасных клеток.
Одним из методов уничтожения клеток является вызов ее самоубийства посредством изменения ионного баланса в клетках. К сожалению, когда обычные клетки становятся канцерогенными, в них изменяетсяи метод транспортировки ионов сквозь клеточную мембрану, что делает апоптоз практически невозможным.
Исследователи из Университета Техаса под руководством профессора Джонатана Сесслера создали синтетический переносчик ионов, который сцепляется с хлорид-ионами. Такая молекула окружает хлорид-ион органическим покрытием, что позволяет молекуле растворяться в клеточной мембране, состоящей в основном из липидов.
Ученые обнаружили, что транспортер хлорид-ионов имеет тенденцию использоват натриевые каналы в мембране, по пути присоединяя и натрий.
В это же время профессор Индже Шин из Университета Ионсей с коллегами сумел показать, что такая синтетическая молекула способствует развитию апоптозу культивированных человеческих канцерогенных клеток.
Подробнее
В поисках новых эффективных средств борьбы с раком ученые обратили внимание на перекись водорода, так как это средство успешно используется в различных областях медицины. Американскими специалистами открыта молекула, способная существенно повлиять на раковые клетки. В частности, она может блокировать механизм, который позволяет клеткам рака в мышином организме противостоять губительным для них кислородным соединениям.
Эксперты придают огромное значение данному открытию. Благодаря полученным результатам ученые могут начать разрабатывать уникальные методы лечения, эффективные при немелкоклеточном раке легких.
Как выяснили специалисты, процесс развития онкологических опухолей сопровождается выделением большого количества химических соединений агрессивного характера. Это так называемые АФК (активные формы кислорода). Чтобы не подвергнуться губительным воздействиям этих соединений, клетки рака запускают особый механизм, синтезирующий белки-антиоксиданты, которые способны нейтрализовать АФК.
Если точнее, то перекись водорода. По мнению многих ученых медиков, создание блокаторов антиоксидантов может стать очень перспективным направлением и откроет новые возможности. Лекарственная терапия рака в таком случае пополнится эффективными средствами.
Эксперименты ставились на мышах в условиях лаборатории. Что касается людей, то среди прочих онкологических болезней на рак легких данной формы приходится примерно восемьдесят пять процентов. То есть, большинство пациентов подвержены именно немелкоклеточному раку легких. Ученые рассказали, что были немало удивлены, когда обнаружили свойства молекулы, которая причислена к аналогам тетрамолибдатов.
Сейчас имеется надежда создания практически уникального метода, который будет использоваться для лечения немелкоклеточного рака. Эксперимент на мышах позволил убедиться, что действительно под воздействием молекулы на раковую опухоль, она в самом деле уменьшилась, причем, значительно.
В научном обществе данная технология признана перспективной и заслуживающей особого внимания. Ученые планируют продолжить работу в данном направлении, и найти дополнительные подтверждения эффективности методики. Возможно, при таком лечении немелкоклеточный рак легких будет легко побежден.
Подробнее
Группа американских экологов, исследовавшая состав водопроводной воды в тридцати пяти городах страны, обнаружила, что вода практически во всех из них (за исключением четырех населенных пунктов) содержит большое количество химических веществ, обладающих канцерогенными свойствами.
В частности, это относится к шестивалентному хрому, содержание которого превысило отметку допустимой нормы в пробах, полученных в 25 городах. Способность хрома провоцировать онкологические заболевания была доказана еще в 2008 году.
Как отмечают ученые, при попадании в организм данное вещество может способствовать возникновению негативных процессов во многих внутренних органах, в частности, в молочных железах, а при вдыхании его пары могут приводить к развитию рака легких. Недавно состоявшаяся проверка обусловлена тем, что в настоящее время Федеральная служба защиты окружающей среды и Национальные институты здравоохранения ведут борьбу с содержанием данного химического соединения в водопроводной воде.
В воде небольшое количество шестивалентного хрома может появляться в результате выщелачивания в грунтовые воды из природных руд. Однако катастрофические масштабы приняла утечка вещества, случившаяся несколько лет назад по вине одной из промышленных компаний штата Калифорния.
Тогда руководству организации пришлось выплатить пострадавшим компенсацию в размере 333 миллионов долларов. Кроме того, вещество до сих пор применяется при производстве различных видов пластмасс и некоторых красителей.
Подробнее
Британские исследователи обнаружили новое средство, которое может совершить настоящий прорыв в области лечения онкологических заболеваний.
Группе специалистов Кембриджского университета удалось определить механизм, в соответствии с которым раковые клетки защищают себя от воздействия иммунной системы женского организма, а также то, как предотвратить его действие.
Оказалось, что защита раковых клеток от уничтожения достигается благодаря выработке специфического белка. Его подавление, напротив, существенно увеличивает шансы на успешное излечение от опухоли молочной железы.
Как пояснил ведущий автор исследования, профессор иммунологии Дуглас Ферон, к настоящему моменту медики провели соответствующие испытания на лабораторных крысах, однако подобные закономерности действуют и в женском организме.
Так, в ходе лабораторных опытов, медики обнаружили существование особого белка (альфа-белка, способствующего активации фибропластов). Данный белок стимулирует защитные силы иммунитета при ранах, ускоряя исцеление поврежденных клеток и тканей.
Однако раковые клетки воспринимаются данными молекулами также как поврежденные и, вместо того, чтобы уничтожать их, белок, наоборот, питает опухоль. У генетически модифицированных грызунов, у которых отсутствовал данный белок, раковые клетки быстро погибали.
По мнению доктора Ферона, на основе полученных данных медики в скором времени смогут создать эффективное лекарство от рака груди.
Подробнее
Оказывается, лекарство от некоторых видов рака можно найти прямо на обеденном столе. Это утверждает. Хуан-Че Чжан, профессор микробиологии и иммунологии в Университете Луисвилля.
В этом фрукте содержатся клетки, которые можно использовать для выработки противораковых антител. В результате экстракции липидов грейпфрута получают наночастицы под названием нановекторы. Именно они служат безопасными проводниками противораковых антител для лечения.
Руководитель исследования опубликовал полученные результаты на прошлой неделе в научном журнале Communications. Здесь же были изложены результаты, полученные в ходе пробного лечения рака толстой кишки.
Исследование показало, что у пациентов не отмечалось никаких токсичных эффектов (например, тошноты, усталости, повышенной утомляемости) во время лечения, и что использование наночастиц грейпфрута была менее вредно, чем все остальные естественные способы лечения этого страшного заболевания.
Чжан уверен, что это лечение абсолютно безрисковое, поскольку проходит через естественные липиды, в отличие от синтетических, которые в настоящее время наиболее распространены.
На вопрос, почему он считает, что грейпфрут может помочь в лечении рака, Чжан сообщил, что информация о пользе фруктов и овощей передается из поколения в поколение.
Подробнее
Группа ученых из Абердинского университета обнаружила, что типичные вредные привычки, в частности, курение, употребление спиртных напитков, а также неправильный рацион питания, увеличивают вероятность появления опухоли полости рта приблизительно в два раза. Известно, что данное заболевание получает все большее распространение среди молодых людей.
В исследовании, которое проводилось в течение пяти лет, приняли участие 350 здоровых девушек и 400 представительниц прекрасного пола, у которых был диагностирован рак. Оказалось, что почти девять из десяти случаев онкологических заболеваний полости рта напрямую связаны с регулярным курением, частым употреблением алкоголя и практически полным отказом от фруктов.
Как отмечает руководитель работы профессор Гари Макфарлейн, эти факторы оказывают негативное влияние и в отношении увеличения риска появления опухолей в других органах, но особенное беспокойство вызывает распространение проблем с верхней частью пищеварительного тракта среди женщин и мужчин моложе 50 лет.
Данные пока являются предварительными, и ученые планируют продолжать работу над исследованием этого вопроса. По их мнению, помимо алкоголизма, курения и неправильного питания, большое значение могут иметь перенесенные ранее инфекционные заболевания, а также генетическая предрасположенность.
Также есть сведения, что появлению подобных опухолей может способствовать длительно пребывание на солнце или неудачно подобранные зубные протезы, вызывающие постоянное раздражение слизистой.
Подробнее
Исследователи из Университета Барселоны синтезировали соединение, которое, по их утверждению отенциально может стимулировать апоптоз широкого спектра линий канцерогенных клеток. Согласно результатам исследования, недавно опубликованным в журнале Angewandte Chemical International Edition, новая молекула воздействует на прохибитин, белок, вовлеченный в различные клеточные процессы и заболевания, в частности, в процессы равития опухолей. также ученые верят, что новые данные представляют потенциал для разработки инновационных терапевтических стратегий лечения рака и открытй новых лекарственных антираковых препаратов.
Исследование было проведено с участием нескольких групп под руководством доктора Родольфо Лавилла, профессора Джоан Джил и профессора Фернандо Альберисио.
Трифторированный тиазолин стал новым соединением, показавшим определенный потенциал в стимулировании апоптоза, или запрограммированной клеточной смерти, в линиях канцерогенных клеток. Для того, чтобы изучить механизм, позволяющий данным молекулам индуцировать апоптоз, исследователи иентифицировали ключевые для него протеины. Проведенное исследование показало, что синтезированные молекулы способны ингибировать функции прохибитинов, которые играют важную роль в пролиферации и апоптозе клеток. Исследователи указывают на то, что синтезированные молекулы могут стать первыми соединениями, после которых последуют и другие с улучшенными свойствами относительно ингибирования прохибитинов.
Существуют некоторые натуральные соединения, сцепленные с прохибитинами, однако, сложность таких соединений и их доступность препятствуют их применению в биологических исследованиях и терапевтических вмешательствах. Приготовление же новых молекул является более доступнымм в связи с чем они могут быть использованы в биологических и медицинских химических программах. Они достаточно стабильны и обладают инновационным каркасом.
Подробнее
Исследователи из Университета Мичигана описали инновационный подход относительно обнаружения потенциальных методов лечения онкологических заболеваний, которые требует меньшего времени по сравнению с традиционными техниками.
Они использовали платфрму для идентификации инновационных антител, которые являлись предметами изучения относительно их потенциального использования в лечении рака груди, рака яичников и других типов онкологических заболеваний.
Результаты исследования были опубликованы в журнале Proceedings национальной академии наук; оно было проведено в лаборатории доктора Стивена Вайсса. Под его руководством исследователи применили инновационный подход, воспроизводящий естественную раковую среду и повышающий вероятность того, что препараты с доказанной эффективность относительно роста клеток опухоли в лабораторных исследованиях также могут остановить рост опухоли и в организме человека. Ученые применили свой метод для идентификации антитела, которое способно остановить рост опухоли при раке груди не только на животной модели, но и у человека.
По утверждению доктора Вайсса, открытие новых целей для онкологического лечения занимает достаточно много времени, а разработка потенциальных лекарственных средств с повышенной специфичностью является сложной задачей. Инновационный подход позволяет определить потенциальные терапевтические цели.
Исследователи сначала создали трехмерную коллагеновую матрицу, которая подобна соединительной ткани, окружающей клетки опухоли при раке груди у людей; далее они интегрировали раковые клетки в полученную матрицу, чтобы набюдать их рост, аналогичный росту в человеческой ткани.
Затем полученный композит былл введен мышам, организм которых опознавал человеческие раковые клетки как чужеродную ткань, в связи с чем их иммунная система начала генерировать тысячи антител для брьбы с человеческими раковыми клетками. В дальнейшем такие антитела были протестированы касательно их способности оостанавливать рост клеток онкологических опухолей.
Подробнее
Недавно ученые выяснили, что эффективность иммунотерапии рака имеет определенную связь с наличием у пациентов конкретных генов. В ходе научной работы был применен препарат Ipilimumab, он способен чаще предотвращать рецидивы, если больные имеют высокую экспрессивность генов, имеющих связь с иммунитетом.
Данным исследованием были охвачены тридцать два пациента, с диагнозом меланома третьей стадии. До того, как была проведена терапия данным препаратом, а также после нее, была проведена биопсия опухоли, выполнен генетический анализ. Эти исследования дали возможность определить уровень активности в трансформированных клетках определенных генов.
Каждый из пациентов, принявший участие, получил хирургическую помощь в полном объеме, им был обеспечен необходимый уход, велось тщательное медицинское наблюдение. Как выяснили ученые, у разных пациентов риск рецидива оказался различен. В частности, если до начала лечения, или непосредственно после его проведения было выявлено наличие высокого уровня экспрессии генов, отвечающих за иммунитет, то после операции риск рецидива рака понижался на шестьдесят три процента.
Ведущие специалисты отмечают, что в современной терапии рака, и в частности, меланомы, достигнут этап, когда имеются максимально высокие результаты. Они обусловлены применением персонализированной медицины, которая основана на генетическом тестировании пациентов.
Не секрет, что лечение рака довольно дорогостоящее, и при этом возникают значительные побочные эффекты. В связи с этим индивидуальному подходу уделяется первостепенное значение. Он определяет не только необходимость лечения, но и его длительность, чтобы минимизировать возможные негативные последствия, уменьшить дополнительные расходы на медикаменты, не являющиеся эффективными.
Данное исследование не является первым, ранее учеными уже проводились эксперименты, определяющие иммунологические маркеры меланомы, прогноз терапии. Теперь известно, что благодаря генетическим маркерам прогноз может быть составлен еще до того, как начнется терапия. В настоящее время установлен ряд некоторых генетических маркеров, необходимых при выборе тактики лечения.
Пока эта работа не представляет собой полноценное эпидемиологическое исследование, поэтому индивидуальный подход следует применять к большому количеству пациентов. Таким образом, стандартизируются генетические анализы, являющиеся наиболее информативными в области терапии меланомы.
Подробнее
Компания InSilico и ее партнеры обеспечили новую яркую наглядную карту, которая позволяет ученым и исследователям лучше понять состояние миелоидных клеток-супрессоров, а также значение их возможной инфильтрации.
Ученые смогли успешно разработать визуализацию молекулярного пути прогрессирования рака, связанного с миелоидными клетками-супрессорами. Причины повреждения и иммунного подавления клеток до сих пор оставались неясными, в связи с чем именно последнее исследование стало важным шагом на пути решения данной проблемы.
Миелоидные клетки-супрессоры появляются в связи с действием опухолевых факторов из клеток-предшественников в гематопоэтических органах, например, костном мозге и, возможно, селезенке. Популяция таких клеток подавляет активность различных ипов иммунных клеток и стимулирует прогрессирование опухоли посредством ангиогенеза и метастаза.
Однако, ключевые транскрипционные регуляторы миелоидных клеток-супрессоров к настоящему времени были не определены. Ученые использовали биоинформатические инструменты, чтобы изучить молекулярный путь интерактомной карты моделей рака кишечника и рака груди.
Были идентифицированы несколько биологических путей, связанных с пролиферацией и распространением раковых клеток при инфильтрации миелоидных клеток-супрессоров. По мнению исследователей, полученные новые результаты могут оказаться полезными в разработке инноваионным методов лечения онкологических заболеваний, целью воздействия которых будут являться именно миелоидные клетки-супрессоры.
Подробнее