Создана новая синтетическая аминокислота для лечения рака и других заболеваний
Одной из наибольших трудностей в современной медицине является то, что разработка и создание лекарственных препаратов с высокой степенью эффективности и с минимальным уровнем токсичности без наличия серьезных побочных эффектв не всегда возможна.
Такие характеристики лекарственных средств напрямую связаны с трехмерной структурой молекулы препарата. В идеале препарат длжен обладать такой формой, которая бы идеально подходила к намеченной цели, на которую он и должен воздействовать, поскольку это повышает высокий уровень сцепления молекул, зависящий от их обоюдной специфичности.
Результаты нового исследования были опубликованы в журнале nature Chemistry, они описывают разработку новой синтетической аминокислоты, которая встроена в трехмерную структуру биоактивных пептидов для увеличения их ппотенциала.
Многие применяемые на сегодняшний момент лекарственные средства являются естественными пептидами и протеинами, они построены на основе аминокислот, обнаруженных в живых организмах. Несмотря на довольно большое разнообразие пептидов и протеинов, все же количество аминикослот ограничено двадцатью видами, каждый из которых обладает уникальнойструктурой и химическими свойствами. При соединении анинокислот в единую последовательность пполучаются пептиды и протеины с различными трехмерными структурами и различными биологическими функциями.
До настоящего времени подавляющее большинство препаратов на основе аминокислот являлись натуральными, например, гормон инсулин, антибиотик ванкомицин, иммунносупрессивное средство циклоспорин. Однако, растущее количество заболеваний выявило насущную необходимость в разработке новых более эффективных препаратов, к примеру, из-за увеличивающегося количества штаммов бактерий, резистентных к действию антибиотиков.
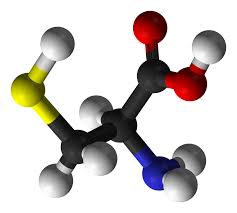
Ученые под руководством доктора Кристиана Хайниса разработали синтетическую аминокислоту с уникальной структурой, которая значительно повышает эффективность терапевтических пептидов и протеино. Она обладает структурой, подобной естественной аминикислоте цистеину, которая в свою очередь, содержит сульфурную группу. А это позволяет ей формировать мостики с другой молекулой цистеина и создавать, таким образом, трехмерную структуру.
Были созданы пять вариантов синтетической аминикислоты, которая в отличие от естественной могла образовывать не один сульфидный мостик, а два. После этого синтетическая аминикислота была интегрирована в структуру двух биоактивных пептидов, один из которых ингибирует энзим, связанный с развитием рака, а другой бллокирует рецептор, обнаруженный в нейронах.